Alles zu Atemschutzmasken
Atemschutzmasken, wie alle Masken umgangssprachlich genannt werden, unterscheiden sich stark in ihren Eigenschaften und ihrer Schutzwirkung. Kein Wunder, dass es – gerade während der Corona-Pandemie – zu vielen Fragen und Unsicherheiten kommt. Auch weil aktuell Privatpersonen ohne medizinischen Hintergrund auf Atemschutzmasken wie FFP2 Masken angewiesen sind.
Wir von nordiska haben die wichtigsten Fragen zu einem Guide zusammengefasst:
- Die wichtigsten Fragen rund um Atemschutzmasken kurz & knackig
- Atemschutzmaske: Persönliche Schutzausrüstung oder Medizinprodukt?
- Übersicht der Filterklasse und Empfehlung für Atemschutzmasken
- Wie prüfe ich die Echtheit & Zertifikation von Atemschutzmasken?
- Was bedeutet non medical für Atemschutzmasken?
Die wichtigsten Fragen rund um Atemschutzmasken kurz & knackig
Welche Atemschutzmaske schützt mich als Träger sowie Dritte?
Nur FFP-Masken, also filtrierende Halbmasken ohne Filter, schützen den Träger sowie sein Gegenüber vor möglichen Infektionen. Die Zahl hinter FFP sagt aus, wie stark die Filterleistung ist:
- FFP1 mindestens 80%,
- FFP2 mindestens 94%
- FFP3 mindestens 99%.
Aufgrund der hohen Filterleistung empfehlen wir für Eigen- sowie Fremdschutz das Tragen von mindestens FFP-2 Masken.
Welche Atemschutzmasken schützen Andere?
Chirurgische Masken oder OP-Masken sind zum Schutz von Patienten konzipiert. Sie schützen Dritte zuverlässig – bei ordnungsgemäßem Gebrauch. Hingegen gewährleisten sie keinen Eigenschutz vor Infektionen, wie dem Corona-Virus.
Schützen FFP-Masken mit Ventil zuverlässig?
FFP-Masken mit Filter bieten nur dem Träger einen zuverlässigen Schutz. Dank des Ventils fällt das Ausatmen leichter, jedoch gelangt die ausgeatmete Luft ungefiltert nach außen. Aerosole können sich so verbreiten, Dritte sind somit leider nicht geschützt. FFP-Masken mit Ventil dienen demnach lediglich dem Selbstschutz.
Wie oft und wie lange dürfen FFP-2 Masken getragen werden?
FFP-2 Masken sind für den einmaligen Gebrauch konstruiert. Die Hersteller empfehlen eine Tragedauer von maximal 8 Stunden. Wird eine Atemschutzmaske durch die Atmung feucht, sollte sie bereits vorher ausgetauscht werden.
Können chirurgische Masken oder FFP-Masken desinfiziert werden?
Wie werden Atemschutzmasken richtig getragen?
Alle Atemschutzmasken verbindet, dass sie sowohl Mund als auch die Nase bedecken müssen, um einen Eigenschutz sowie Fremdschutz zu gewährleisten. Gerade bei FFP-2 und FFP-3 Masken hängt der Schutz auch davon ab, wie dicht die Masken sitzen. Sie sollten den Mund- und Nasenbereich komplett bedecken und lückenlos abschließen.
Woran können sichere und zertifizierte Atemschutzmasken erkannt werden?
- Chirurgische Masken oder OP-Masken entsprechen demnach der der europäischen Norm EN 14683:2019-10
- FFP-Masken genügen der Norm EN 149:2001+A1:2009
Weitere Prüfkriterien können Sie hier nachlesen: Wie prüfe ich die Echtheit & richtige Kennzeichnung von Atemschutzmasken?
Atemschutzmaske: Persönliche Schutzausrüstung oder Medizinprodukt?
Bei diesen Schutzmasken handelt es sich um Medizinprodukte:
Ein chirurgischer Mundschutz ist ein Medizinprodukt: Per Definition dient ein Medizinprodukt immer dem Schutz und der Sicherheit des Patienten. Dementsprechend sind auch die Anwendungsempfehlungen. Der chirurgische Mundschutz wird verwendet, um Patienten unter anderem vor Tröpfchen und Aerosole zu schützen – weniger, um den Träger zu schützen.
Welche Schutzmasken schützen Andere?
- Chirurgischer Mundschutz Typ 2 und Typ 2r
- Chirurgischer Mundschutz zum Binden
Definition Medizinprodukt
Die genaue Definition des Begriffs „Medizinprodukt (MP)“ ist im § 3 MPG zu finden. Darin wird konkret festgelegt, wann ein MP als solches zu bezeichnen ist. Medizinprodukte sind demnach „alle einzeln oder miteinander verbunden verwendete Instrumente, Apparate, Vorrichtungen, Software, Stoffe und Zubereitungen aus Stoffen oder andere Gegenstände einschließlich der vom Hersteller speziell zur Anwendung für diagnostische oder therapeutische Zwecke bestimmten und für ein einwandfreies Funktionieren des Medizinprodukts eingesetzten Software. Sie dienen folgenden Zwecken:
- Erkennung, Verhütung, Überwachung, Behandlung oder Linderung von Krankheiten
- Erkennung, Überwachung, Behandlung, Linderung oder Kompensierung von Verletzungen oder Behinderungen
- Untersuchung, Ersetzung oder Veränderung des anatomischen Aufbaus oder eines physiologischen Vorgangs
- Empfängnisregelung
Risikoklassen
- Klasse I
- geringes Risiko
- geringer Invasivitätsgrad
- vorübergehende Anwendung (< 60 Minuten)
- Beispiele: Gehhilfen, Stützstrümpfe, Verbandmittel
- Klasse IIa
- mittleres Risiko
- mäßiger Invasivitätsgrad
- kurzzeitige Anwendung (< 30 Tage), ununterbrochen / wiederholter Einsatz des gleichen Produkts
- Beispiele: Desinfektionsmittel (für Instrumente und Geräte), Einmalspritzen, Hörgeräte
- Klasse IIb
- erhöhtes Risiko
- systemische Wirkung
- langzeitige Anwendung (> 30 Tage)
- Beispiele: Beatmungsgeräte, Defibrillatoren, Kondome
- Klasse III
- hohes Risiko
- unmittelbare Anwendung an Herz, zentralem Kreislauf- oder Nervensystem
- implantierbar und/oder hoch-invasiv
- Beispiele: Herzkatheter, Stents, künstliche Gelenke
Risikoklassen sind EU-weit durch den Anhang IX der Richtlinie 93/42/EWG festgelegt. Ausnahmen bilden lediglich In-vitro-Diagnostika und aktive implantierbare MP. Die Einteilung in eine Risikoklasse obliegt dem Hersteller mit der Zweckbestimmung. Weder die EU-Richtlinie noch die nationale Gesetzgebung nimmt eine solche Einteilung vor.
PSA - Persönliche Schutzausrüstung
Risikoklassen
Unterschiedliches Risiko – unterschiedliche Anforderungen: Die Anforderungen an Produkte und dessen einmalige oder permanente Prüfung richten sich nach der Kategorisierung in drei Risikogruppen:
Von geringem Risiko für den Träger, wie z.B. bei einfachen Arbeitshandschuhen, bis hin zu hohen Risiken, wie z.B. bei Atemschutzmasken.
Eine Übersicht finden Sie hier:
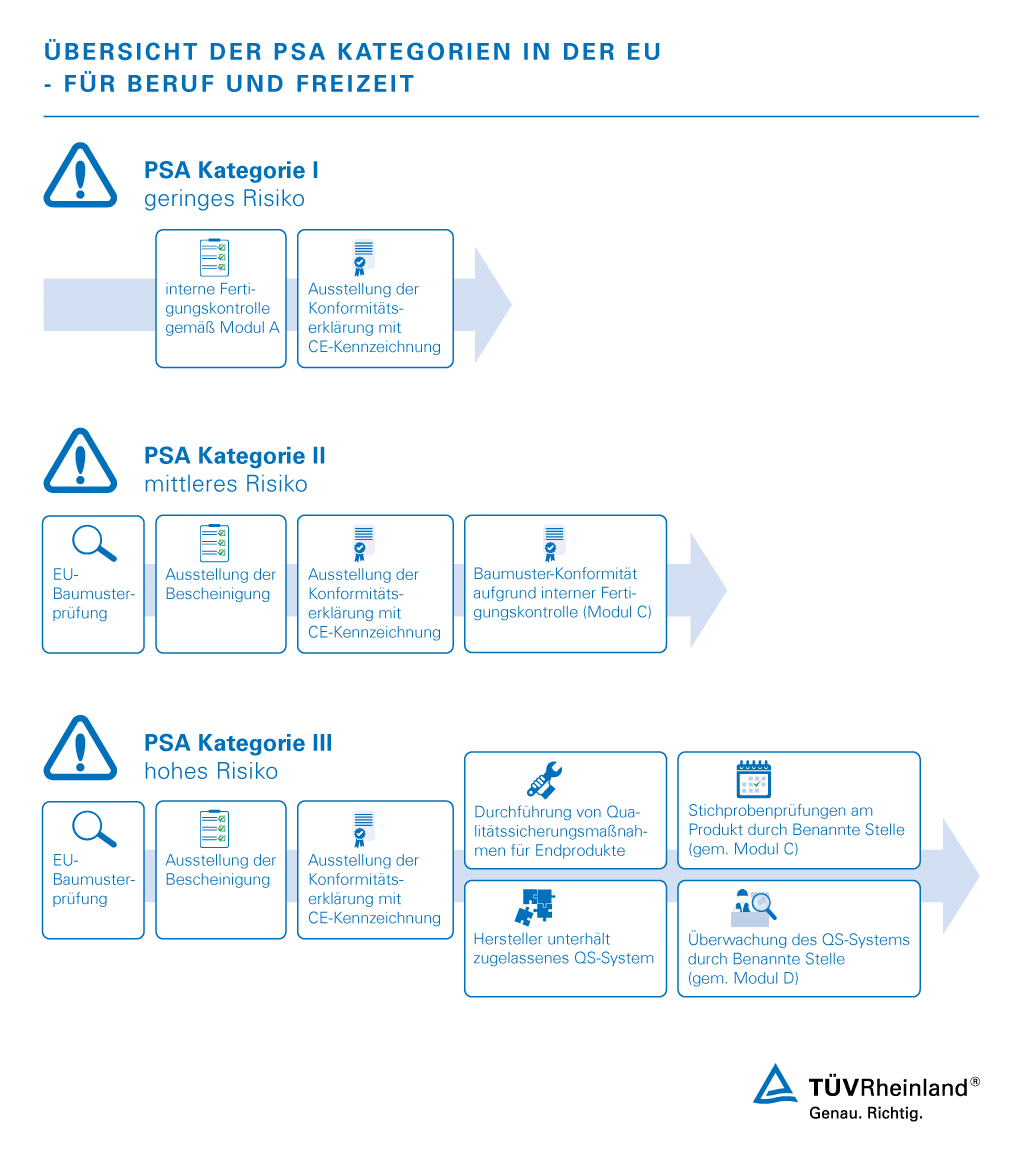
Während einer Pandemie, wie der aktuellen Corona-Pandemie, sind das vor allem:
- FFP1 Masken mit und ohne Ventil
- FFP2 Masken mit und ohne Ventil
- FFP3 Masken mit und ohne Ventil
- Isolationskittel
- Schutzanzüge
Welche Bestimmung zur Kennzeichnung von Atemschutzmasken gilt aktuell?
Zu Beginn der Corona-Pandemie im März 2020 war die Marktnachfrage nach Atemschutzmasken so hoch, dass es zu einer extremen Knappheit kam. Dadurch wurde von der EU-Kommission eine vereinfachte Sonderzulassen in Kraft gesetzt, die es ermöglicht hat, diesen Engpass zu überbrücken.
Kein Wunder, dass eine Unsicherheit herrscht, welche Bestimmung aktuell gilt und welche Kennzeichnungen auf Masken zuverlässigen Schutz gewährleisten. Ein chronologischer Überblick:
Vereinfachte Sonderzulassung – gültig bis 31.08.2020:
Dank vereinfachter EU-Bestimmungen konnten ab dem 13.03.2020 fehlende PSA-Produkte unkompliziert und schnell importiert und in Verkehr gebracht werden.
Dies galt vor allem für die so dringend benötigten filtrierenden Halbmasken. Hiernach war es für einen begrenzten Zeitraum möglich, Schutzmasken, die nicht nach der Norm EN149:2009+A1:2009 geprüft waren, in Umlauf zu bringen.
Dabei handelt sich um so genannte CPA: Corona Virus Pandemie Atemschutz-Masken.
Bedingungen hierfür waren:
- Ausgabe ausschließlich an medizinische Fachkräfte für einen begrenzten Zeitraum.
- Ohne CE Kennzeichnung ist dann zulässig, wenn die Masken in den USA, Kanada, Japan oder Australien entsprechend der dort gültigen Normen geprüft wurden.
- Ohne CE Kennzeichnung aus Drittländern ist zulässig, allerdings müssen diese Masken einem Schnelltest entsprechend der Vorgaben der ZLS (Zentralstelle der Länder für Sicherheitstechnik) unterzogen werden und diesen bestehen.
Ein besonderes Augenmerk liegt hierbei auf der vereinfachten Sonderzulassung ungekennzeichneter Ware aus Drittländern: Die durch einen Schnelltest zugelassene Ware wurde auf Basis der für Medizinprodukte gültigen Prüfnorm EN: 14863:2019+AC2019 zugelassen. Die entsprechenden Produkte wurden maßgeblich durch das Bundesinstitut für Arzneimittel und Medizinprodukte, kurz BfArM, kontrolliert und dokumentiert.
Aktuelle Anforderungen – gültig seit Juli 2020:
Das BfArM hat Ende Juni 2020 festgestellt, dass es für medizinische Schutzmasken keinen Versorgungsengpass mehr gibt. Eine Sonderzulassung, die das Interesse der öffentlichen Gesundheit oder der Patientensicherheit rechtfertigen, ist demnach nicht mehr gültig.
Sonderzulassungen auf Basis bereits vorliegender Anträge wurden bis spätestens dem 31.08.2020 befristet. Dies gilt für Anträge, die bis zum 30.06.2020 eingegangen sind. Folgeanträge wurden nicht mehr berücksichtigt.
In der Folge könnten nicht CE-gekennzeichnete medizinische Gesichtsmasken und FFP-Masken künftig nicht mehr auf der Grundlage von Sonderzulassungen in Deutschland bereitgestellt werden.
Wichtig hierbei: Bereits eingeführte Ware kann weiterhin verwendet und verkauft werden. Ab dem 31.08.2020 ist allerdings die Einfuhr von PSA- Produkten nur noch mit einer nachweisbaren und gültigen Konformität zu den in der EU gültigen Normen und Grundsätzen möglich.
Übersicht der Filterklasse und Empfehlung
Oftmals sind unsere Kunden verwirrt bzgl. der unterschiedlichen Normen, Filterklassen und Prüfstandards.
Atemschutzmasken-Klassen auf einen Blick
| Maskentyp | Standard | Filtereffektivität / Maskenklassifizierung | ||
|---|---|---|---|---|
OP Masken 
| Europa: EN 14683 | Typ I | Typ II | Typ II R |
| BFE: ≥ 95% | BFE: ≥ 98% | BFE: ≥ 98% | ||
| PFE: k.A. | PFE: k.A. | PFE: k.A. | ||
| USA: ASTM F2100 | Level 1 | Level 2 | Level 3 | |
| BFE: ≥ 95% | BFE: ≥ 98% | BFE: ≥ 98% | ||
| PFE: ≥ 95% | PFE: ≥ 98% | PFE: ≥ 98% | ||
| China: YY 0469 | BFE: ≥ 95% PFE: k.A. | |||
Feinstaubmasken 
| Europa: EN 149:2001 | FFP1 | FFP2 | FFP3 |
| 0,6 µm ≥ 80% | 0,6 µm ≥ 94% | 0,6 µm ≥ 99% | ||
| USA: NIOSH (42 CFR 84) | N95 | N99 | N100 | |
| 0,3 µm ≥ 95% | 0,3 µm ≥ 99% | 0,3 µm ≥ 99,7% | ||
| China: GB2626 | KN95 | KN99 | KN100 | |
| 0,3 µm ≥ 95% | 0,3 µm ≥ 99% | 0,3 µm ≥ 99,7% | ||
| BFE: Bakterielle Filterleistung PFE: Partikelfilterleistung µm = Mikrometer | 
| |||
Hier ist deutlich die Unterscheidung zwischen OP-Masken und Feinstaubmasken als persönliche Schutzausrüstung zu erkennen.
OP - oder chirurgische Masken
Chirurgische Masken sind für den Schutz des Patienten konzipiert. OP-Masken, wie sie auch genannt werden, werden demnach als Medizin-Produkt kategorisiert. Maßgeblich ist die Vorgabe der Prüfnorm EN 14683:2019 + AC 2019. Neben weiteren Vorgaben zum Atemwiderstand und einer Grenze für lose Partikel, steht vor allem die bakterielle Filterleistung im Vordergrund.
- Bei Typ 1 Masken beträgt diese mindestens 95%
- bei Typ 2 Masken mindestens 98%.
Es geht bei diesen Produkten vor allem darum, dass der Patient vor Partikeln und Bakterien in einer OP-Situation geschützt ist. Es geht also nicht um eine zuverlässige Filterleistung gegen Viren und Aerosole für den Träger.
- Beim Typ 2r ist eine zusätzliche Flüssigkeitsresistenz, welche durch einen zusätzlichen Spritztest mit synthetischem Blut geprüft wird, entscheidend. Der Atemwiderstand darf hierbei dann aber auch 60 PA/cm² betragen.
nordiska Empfehlung zum Tragen von chirurgischen Masken im Alltag:
OP-Masken sind im täglichen Umgang ein sinnvoller Schutz vor Tröpfcheninfektionen. Im Gesundheitswesen können diese ebenfalls überall dort eingesetzt werden, wo keine akute Vermutung eines infektiösen Patienten besteht, z.B. auf „Normalstation“ nach erfolgtem Schnelltest bei Aufnahme des Patienten.
Unsere klare Empfehlung geht hin zur Maske des Typ2r, um hier zumindest eine Flüssigkeitsresistenz zu gewährleisten.
Filtrierende Halbmasken (FFP)
Filtrierende Halbmasken (FFP) schützen den Träger. Sie wurden als Feinstaubmasken konzipiert und sind als persönlich Schutzausrüstung kategorisiert. In der EU werden sie nach den strengen Richtlinien der PSA- Verordnung (EU) 2016/425 Annex 5 reglementiert.
Bei der Filterleistung wird strikt auf die Partikelgröße geachtet, welche in der EU mit 0,6 Mikrometern gewählt wurde. Dies entspricht Feinstaub und ist zugleich auch so klein gewählt, dass die meisten Viren, Aerosole und Bakterien zuverlässig gefiltert werden. Aus diesem Grunde fiel die Wahl in der aktuellen Pandemie auf diesen Typ der Schutzmaske.
Die Zahlen 1-3 geben hierbei die Prozentzahl der zuverlässig gefilterten Partikel an:- FFP1 mindestens 80%,
- FFP2 mindestens 94%
- FFP3 mindestens 99%.
FFP vs. N – Vergleich der unterschiedlichen Standards:
Ausländische Standards, wie KN & N, sorgen immer wieder für Unklarheit bezüglich der Qualität und Filterleistung. Dabei sind sie mit den FFP-Standards vergleichbar.
Generell sind die Kriterien des chinesischen Standards GB2626:2006 und des amerikanischen NIOSH Standards analog zu unseren europäischen. Aus dem Grund konnten diese Atemschutz-Masken in der Notlage zu Beginn der Corona-Pandemie zugelassen werden.
Bei der Partikelgröße sind beide Standards sogar noch strenger. Unterschiede gibt es allerdings in den Testmethoden. Hier fehlte beim chinesischen Standard z.B. der Filtrationstext mit Parafinöl.
Generell gilt: KN95 oder N95 müssen nicht zwingend schlechter sein als FFP2 Schutzmasken.
Lediglich die fehlende Kontrolle der erzielten Werte durch eine unabhängige Stelle in der EU ist als Manko aufzuführen, denn somit besteht die potenzielle Gefährdung durch Fälschungen und Betrug. Dies ist im europäischen Konformitätsbewertungsverfahren nahezu ausgeschlossen.
Das gilt für die Masken mit und ohne Ventil
Alle drei Klassen sind mit und ohne Ausatemventil erhältlich und auch potenziell angemessen.
>> Allerdings schützen die Masken mit Ventil nur den Träger der Maske.
Masken mit Ventil sollten allerdings nur verwendet werden, wenn davon auszugehen ist, dass weitere beteiligte Personen nicht geschädigt werden können, z.B. bei FFP3 Masken auf einer Corona-Station.
Selbst bei zertifizierten Masken mit Ventil können in Einzelfällen durch falsche Lagerung, eine Beschädigung auf dem Transportweg oder durch andere Gründe Problemen mit dem Verschluss der Membran im Ventil entstehen. Eine Maske ohne Ventil hat diese „Schwachstelle“ nicht.
Zusammengefasst bedeutet das:
- Masken ohne Ventil schützen Träger und weitere Beteiligte.
- Masken mit Ausatemventil schützen nur den Träger der Maske, da die Atemluft beim Ausatmen ungefiltert die Maske verlässt.
nordiska Empfehlung:
- FFP2: Überall, wo ein Kontakt zu potenziell infizierten Personen zu vermuten ist (Ambulanz, OP, usw.) empfehlen wir eine FFP2 Atemschutzmaske. Hier ist eine hohe Gewährleistung der Sicherheit des Trägers gegeben und der Tragekomfort (Atemwiderstand, Passform, etc.) ist auch über einen längeren Zeitraum „erträglich“.
- FFP3: Überall, wo mit infizierten Patienten gearbeitet wird, empfehlen wir zwingend eine FFP3 Schutzmaske.
Wie prüfe ich die Echtheit & richtige Kennzeichnung von Atemschutzmasken?
Unterschiedliche Kategorien = unterschiedliche Zertifikate. Atemschutzmasken, die unter die Kategorie Medizinprodukt fallen, haben andere Zertifikate & Prüfkriterien als Atemschutzmasken, die einer persönlichen Schutzausrüstung entsprechen.
Das sind die vereinfachten Unterschiede zwischen beiden Kategorien:
- Medizinprodukte schützen Patienten
- Persönliche Schutzausrüstung schützt den Träger (meistens auch den Patienten)
Wichtigste Prüfkriterien von Atemschutzmasken der Kategorie Medizinprodukte
Die derzeit stark nachgefragten Produkte im Zusammenhang mit der Corona- Pandemie sind vor allem 3-lagiger Mundschutz Typ2 und Typ 2r zur Prävention von Tröpfchen-Übertragungen und diverse Stations- und Besucherkittel.
Diese Produkte bieten alle keinen zuverlässigen Schutz gegen eine Infektion und sollten nur präventiv in Bereichen eingesetzt werden, in denen eine Infektion möglich ist. Diese Produkte (sofern nicht steril) sind alle der Medizinproduktklasse 1 zuzuordnen.
Nordiska als Händler prüft hier die folgenden Unterlagen, um eine Konformität mit den in der EU geltenden Normen und somit eine CE Kennzeichnung des Produktes zu gewährleisten:
- EG Konformitätserklärung unter Angabe von:
- Des EG Repräsentanten (EC Rep.)
- Der angewandten Prüfnorm
- Des Herstellers
- Ordnungsgemäße Kennzeichnung der kleinsten Verpackungseinheit
- Aufdruck CE Kennzeichnung
- EU Repräsentant mit Adresse, E-Mail-Adresse oder Telefonnummer
- LOT- Nummer
- Produktionsdatum
- Ablaufdatum
- Einen Testbericht der angewandten Prüfnorm
- Einem ISO 13485:2016 Zertifikat des Produzenten
Als Kunde sollten Sie vor Kauf zwingend nach der EG Konformitätserklärung fragen und sich diese zuschicken lassen, um die Konformität des Produktes zu überprüfen. Die weiteren Dokumente müssen Ihnen der Händler oder Produzent nicht zwingend zur Verfügung stellen.
Wir bei nordiska geben unseren Kunden immer alle uns vorliegenden Dokumente an die Hand.
Wichtigste Prüfkriterien von Atemschutzmasken der Kategorie Persönliche Schutzausrüstung
Gerade Schutzausrüstung, die den Träger vor einer Infektion mit SARS-CoV-2 schützt, sind derzeit stark nachgefragt. Sie sind der persönlichen Schutzausrüstung Klasse II zuzuordnen und unterliegen besonderen Bedingungen:
Ab dem 31.August 2020 ist die Einfuhr von PSA- Produkten nur noch mit einer nachweisbaren und gültigen Konformität zu den in der EU gültigen Normen und Grundsätze möglich.
Betreffende Produkte sind unter anderem:
- Atemschutzmasken der Schutzklasse FFP1, FFP2 und FFP3; jeweils mit und ohne Ventil
- Isolationskittel
- Faceshields oder Gesichtsvisiere
- Untersuchungs- oder Behandlungshandschuhe (Latex, Nitril, Vinyl)
Nordiska als Händler prüft für alle Produkte der PSA Kat. III Unterlagen und verifiziert diese wie folgt, um eine Konformität mit den in der EU geltenden Normen und somit eine CE Kennzeichnung des Produktes zu gewährleisten:
- Verifizierbare EG Baumusterprüfbescheinigung Modul B
Die Baumusterprüfbescheinigung Modul B ist die offizielle Prüfung einer Stelle in der EU und Bestätigung der Testergebnisse (können auch durch ein angeschlossenes Labor in Fernost durchgeführt werden).- Angabe der durchführenden notifizierten Stelle (notified body)
- Angabe des Produktcodes und der entsprechenden Varianten
- Angabe der angewendeten Normen
- Angabe der erreichten Leistungsklassen oder Ergebnissen
- Angabe der Gültigkeit (in der Regel 5 Jahre)
- Möglichkeit zu Verifizierung der Baumusterprüfbescheinigung
Verifizierung:
Alle gängigen notifizierten Stellen führen eine Datenbank mit den ausgestellten Baumusterprüfbescheinigungen, entweder als QR Code oder unter Angabe der URL. Hier ist zwingend unter Eingabe der Zertifikatsnummer zu prüfen, ob die Informationen auf dem Dokument mit denen auf der Baumusterprüfbescheinigung übereinstimmen.Verifizierung der notifizierten Stelle:
Zudem prüfen wir immer anhand der Nummer der zertifizierenden Stelle, ob diese laut Nando Liste https://ec.europa.eu/growth/tools-databases/nando zur Zertifizierung von PSA akkreditiert ist.
- Verifizierbare EG Baumusterprüfbescheinigung Modul B
- Verifizierbare EG Baumusterprüfbescheinigung Modul C2 oder D
Bei PSA der Kategorie III muss aufgrund des hohen Risikos neben der notifizierten Stelle für die EU-Baumusterprüfung (Modul B) auch eine notifizierte Stelle für die Überwachung eingebunden werden.
Für die Überwachung hat der Hersteller die Wahl zwischen:- Konformität mit dem Baumuster auf der Grundlage einer internen Fertigungskontrolle mit überwachten Produktprüfungen in unregelmäßigen Abständen (Modul C2) gemäß Anhang VII;
- Konformität mit dem Baumuster auf der Grundlage einer Qualitätssicherung bezogen auf den Produktionsprozess (Modul D) gemäß Anhang VIII.
Verifizierung:
Wie beim Modul B führen alle gängigen notifizierten Stellen eine Datenbank mit den ausgestellten Baumusterprüfbescheinigungen Modul C2 oder D. Entweder als QR Code oder unter Angabe der URL.
Hier ist zwingend unter Eingabe der Zertifikatsnummer zu prüfen, ob die Informationen auf dem Dokument mit denen auf der Baumusterprüfbescheinigung übereinstimmen.Verifizierung der notifizierten Stelle:
Zudem prüfen wir immer anhand der Nummer der zertifizierenden Stelle, ob diese laut Nando Liste https://ec.europa.eu/growth/tools-databases/nando zur Zertifizierung von PSA akkreditiert ist.
- Verifizierbare EG Baumusterprüfbescheinigung Modul C2 oder D
- EG Konformitätserklärung unter Angabe:
- Der Baumusterprüfbescheinigungen und der notifizierten Stellen Modul B und Modul C2 oder D
- Der angewandten Prüfnorm
- Des Herstellers
- EG Konformitätserklärung unter Angabe:
- Ordnungsgemäße Kennzeichnung der kleinsten Verpackungseinheit
- Aufdruck CE Kennzeichnung mit 4stelliger Nummer der notifizierten Stelle (bei Abweichung Modul B und C2 oder D)
- Inverkehrbringen
- Angewendete Normen
- PSA- Schutzklasse
- Artikelcode
- LOT- Nummer
- Produktionsdatum
- Ablaufdatum
- Ordnungsgemäße Kennzeichnung der kleinsten Verpackungseinheit
- Ordnungsgemäße Gebrauchsanweisung in einer gängigen Sprache (Deutsch oder Englisch) unter Angabe von (kann auch in Form von Piktogrammen erfolgen):
- Lagerungshinweisen
- Entsorgungshinweisen
- Aufbereitungshinweisen bzw. einer Kennzeichnung als Einwegprodukt
- Hinweisen zum korrekten Gebrauch/ Tragen der PSA
- Ordnungsgemäße Gebrauchsanweisung in einer gängigen Sprache (Deutsch oder Englisch) unter Angabe von (kann auch in Form von Piktogrammen erfolgen):
- Einen Testbericht der angewandten Prüfnorm, welcher sich auch auf der Baumusterprüfbescheinigung Modul B wiederfinden sollte.
- Einem ISO 9001 (Qualitätsmanagement) Zertifikat des Produzenten
Alle diese Unterlagen werden von uns eingehend geprüft. Als Kunde sollten Sie vor Kauf zwingend nach der EG Konformitätserklärung fragen und sich diese schicken lassen, um die Konformität des Produktes zu überprüfen. Zudem lassen Sie sich die Verpackung und die Gebrauchsanweisung zeigen und prüfen Sie, ob notifizierte Stelle, Produzent und Artikelangaben mit denen auf der Konformitätserklärung übereinstimmen. Die weiteren Dokumente müssen Ihnen der Händler oder Produzent nicht zwingend zur Verfügung stellen.
Wir bei nordiska geben unseren Kunden immer alle uns vorliegenden Dokumente an die Hand.
Was bedeutet non medical für Atemschutzmasken?
Non Medical ist mit PSA, also einer persönlichen Schutzausrüstung, gleichzusetzen.
Die Masken dürfen ausdrücklich im medizinischen Bereich verwendet werden.
Die Bezeichnung ist etwas irreführend: Sie drückt aus, dass es sich nicht um ein Medizinprodukt handelt, dass ausschließlich den Patienten schützt, sondern dem persönlichen Schutz dient.
Die Angabe dieser Kennzeichnung hängt ausschließlich mit den chinesischen Zollbestimmungen zusammen: Hier hat das chinesische Handelsministerium die Ausfuhr von „Corona- Artikeln“ stark reglementiert, um Plagiaten und Fälschungen entgegen zu wirken.
Seitdem gibt es zwei Whitelists: Eine für Medizinprodukte und eine für Nicht-Medizin/ PSA-Produkte. Nur Unternehmen, die vor Corona diese Artikel exportiert haben, dürfen diese auch weiter exportieren. Da es wiederholt Probleme im chinesischen Zoll gab, weil Masken auf der Medizinprodukt-Whitelist gesucht wurden, gab es hier enorme Verspätungen und Kosten für eine Zollbeschau.
Daher drucken die meisten Produzenten non medical auf das Produkt. So gibt es hier keine Verwechslungen mehr, was den Export vereinfacht. Ausnahme sind Hersteller für Medizinprodukte und PSA- Produkte. Diese sind auf beiden Listen und drucken kein „non medical“ auf.
Verwendung:
Ob mit oder ohne non medical: Derzeit kommen keine PSA-Atemmasken ohne 4-stellige Nummer des notified bodies auf den europäischen Markt. Zudem sollten die entsprechenden Baumusterprüfbescheinigungen und eine Konformitätserklärung vorliegen.
Liegt dies vor und ist die Ware korrekt gekennzeichnet, sind die Masken zur Verwendung als PSA Kat. III geeignet und zulässig. Egal ob im Krankenhaus oder einem Industriebtrieb – sie schützen zuverlässig. Der Aufdruck bezieht sich dabei nur auf die Prüfnorm, nicht auf den Verwendungszweck.
Weil es aufgrund dieses Aufdruckes allerdings immer wieder zu großen Verwirrungen und Unsicherheit bei den Anwendern kommt, vertreiben wir als nordiska ausschließlich Masken ohne non-Medical Aufdruck.


